TD10 Enonce
DownloadTélécharger
Actions
Vote :
ScreenshotAperçu
Informations
Catégorie :Category: mViewer GX Creator Lua TI-Nspire
Auteur Author: Pa Baz
Type : Classeur 3.6
Page(s) : 4
Taille Size: 450.88 Ko KB
Mis en ligne Uploaded: 07/04/2015 - 00:53:08
Uploadeur Uploader: Pa Baz (Profil)
Téléchargements Downloads: 102
Visibilité Visibility: Archive publique
Shortlink : http://ti-pla.net/a184532
Type : Classeur 3.6
Page(s) : 4
Taille Size: 450.88 Ko KB
Mis en ligne Uploaded: 07/04/2015 - 00:53:08
Uploadeur Uploader: Pa Baz (Profil)
Téléchargements Downloads: 102
Visibilité Visibility: Archive publique
Shortlink : http://ti-pla.net/a184532
Description
Philippe APLINCOURT
Master 1 MEEF Physique-Chimie
TD 10
Diagrammes binaires
Séparation de l’éthanol – Extrait CAPES Externe 2007
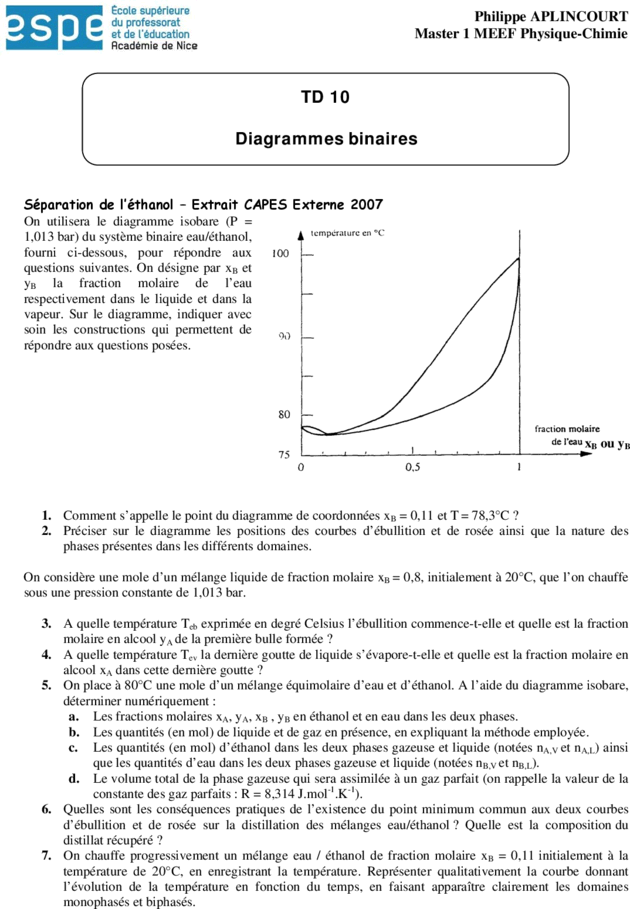
On utilisera le diagramme isobare (P =
1,013 bar) du système binaire eau/éthanol,
fourni ci-dessous, pour répondre aux
questions suivantes. On désigne par xB et
yB la fraction molaire de l’eau
respectivement dans le liquide et dans la
vapeur. Sur le diagramme, indiquer avec
soin les constructions qui permettent de
répondre aux questions posées.
xB ou yB
1. Comment s’appelle le point du diagramme de coordonnées xB = 0,11 et T = 78,3°C ?
2. Préciser sur le diagramme les positions des courbes d’ébullition et de rosée ainsi que la nature des
phases présentes dans les différents domaines.
On considère une mole d’un mélange liquide de fraction molaire xB = 0,8, initialement à 20°C, que l’on chauffe
sous une pression constante de 1,013 bar.
3. A quelle température Teb exprimée en degré Celsius l’ébullition commence-t-elle et quelle est la fraction
molaire en alcool yA de la première bulle formée ?
4. A quelle température Tev la dernière goutte de liquide s’évapore-t-elle et quelle est la fraction molaire en
alcool xA dans cette dernière goutte ?
5. On place à 80°C une mole d’un mélange équimolaire d’eau et d’éthanol. A l’aide du diagramme isobare,
déterminer numériquement :
a. Les fractions molaires xA, yA, xB , yB en éthanol et en eau dans les deux phases.
b. Les quantités (en mol) de liquide et de gaz en présence, en expliquant la méthode employée.
c. Les quantités (en mol) d’éthanol dans les deux phases gazeuse et liquide (notées nA,V et nA,L) ainsi
que les quantités d’eau dans les deux phases gazeuse et liquide (notées nB,V et nB,L).
d. Le volume total de la phase gazeuse qui sera assimilée à un gaz parfait (on rappelle la valeur de la
constante des gaz parfaits : R = 8,314 J.mol-1.K-1).
6. Quelles sont les conséquences pratiques de l’existence du point minimum commun aux deux courbes
d’ébullition et de rosée sur la distillation des mélanges eau/éthanol ? Quelle est la composition du
distillat récupéré ?
7. On chauffe progressivement un mélange eau / éthanol de fraction molaire xB = 0,11 initialement à la
température de 20°C, en enregistrant la température. Représenter qualitativement la courbe donnant
l’évolution de la température en fonction du temps, en faisant apparaître clairement les domaines
monophasés et biphasés.
Philippe APLINCOURT
Master 1 MEEF Physique-Chimie
Equilibre liquide-solide du binaire eau-urée
On donne ci-dessous, le diagramme de cristallisation du binaire eau-urée, sous la pression atmosphérique.
1. Indiquer si l’urée et l’eau sont totalement miscibles ou non miscibles à l’état solide.
2. Nommer les courbes 1 et 2 séparant les différents domaines.
3. Indiquer à quelles compositions correspondent les domaines I à IV.
4. Comment se nomme le point A commun des deux courbes ? Préciser à quel système il correspond.
Un système est constitué d’une masse m1 = 70 g d’urée et d’une masse m2 = 30 g d’eau. Il est porté à 90°C. On
le refroidit régulièrement, sous la pression atmosphérique, jusqu’à une température de -30°C.
5. Tracer l’allure de la courbe d’analyse thermique donnant l’évolution de la température du système en
fonction du temps. Préciser les phénomènes se produisant aux différents points particuliers de la courbe.
Calculer la variance du système pour les domaines où plusieurs phases coexistent.
6. Rechercher la composition et calculer les masses de chaque phase pour une température de 0°C. Donner
la masse d’urée et la masse d’eau de la phase liquide.
Une masse m3 = 10 g d’urée solide pure est portée à -5°C. À pression et température constantes, on apporte petit
à petit une masse m4 = 90 g d’eau au système.
7. Selon la fraction massique globale en urée du système, indiquer la nature des phases en présence et la
fraction massique en urée de l’éventuelle phase liquide.
Philippe APLINCOURT
Master 1 MEEF Physique-Chimie
Mélange cuivre-argent
Dans le cas du mélange argent-cuivre, on observe une solubilité partielle à l’état solide.
On donne les points caractéristiques du diagramme binaire isobare (P = P0) argent-cuivre ; x(Cu) représente la
fraction atomique en cuivre du mélange.
Ag Cu
1400
1300
1200
Température (K)
1100
1000
900
800
700
600
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1
x (Cu)
1. Reproduire schématiquement le diagramme en reliant les points de façon appropriée. Préciser les
espèces (nature et état physique) présentes dans les différents domaines du diagramme ainsi définis et
préciser les coordonnées du point eutectique.
On laisse refroidir lentement un mélange argent-cuivre avec x(Cu) = 0,2 de 1400 K à 800 K.
2. Tracer l’allure de la courbe donnant la température du système en fonction du temps (courbe d’analyse
thermique) et préciser la variance du système au cours de la transformation.
3. Déterminer la composition du système à 1100 K.
On considère un barreau d’argent contenant 10% de cuivre considéré comme une impureté.
4. En vous aidant du diagramme, proposer une méthode de purification du barreau d’argent.
Philippe APLINCOURT
Master 1 MEEF Physique-Chimie
L’alliage aluminium/hafnium
L’aluminium s’allie à de nombreux composés. Sa légèreté et son coût modéré le rendent particulièrement
intéressant pour certaines applications où un poids élevé est un handicap, comme en aéronautique.
Le hafnium a la particularité de ne pas laisser passer les neutrons d’où les applications dans l’industrie
nucléaire pour arrêter les réacteurs. Du fait aussi de sa haute température de fusion, il est utilisé dans les
briques réfractaires. Avec l’aluminium, il rentre dans la composition de nouveaux alliages, comme les alliages
« superplastiques » au zirconium.
On s’intéresse ici au système binaire aluminium / hafnium (de symbole Hf). On désire construire le diagramme
isobare de cristallisation de ce système binaire sachant que les solides sont tous non miscibles entre eux et que
le liquide est homogène. Pour cela, on étudie les courbes de refroidissement de différents mélanges aluminium –
hafnium avec une fraction molaire d’aluminium comprise entre 0,60 et 0,75. Les différentes courbes sont
rassemblées sur la figure ci-dessous.
1. A l’aide de ces courbes, tracer le diagramme binaire isobare T(x) du système aluminium – hafnium pour
une fraction molaire x en aluminium comprise entre 0,60 et 0,75 et une température comprise entre
1480°C et 1720°C.
2. Pour chaque domaine du diagramme binaire, donner la nature des phases en présence. Indiquer le ou les
composés définis trouvés dans cette partie du diagramme binaire.
3. Pour x = 0,62 et x = 0,72, on observe un point particulier. Comment s’appelle ce point ? Quelle
particularité possède le mélange liquide à cette fraction molaire ?
4. Pour les courbes de refroidissement où x = 0,60, x = 0,62 et x = 0,69, décrire ce qu’il se passe, et
calculer la variance du système pour chaque partie de ces courbes.
Master 1 MEEF Physique-Chimie
TD 10
Diagrammes binaires
Séparation de l’éthanol – Extrait CAPES Externe 2007
On utilisera le diagramme isobare (P =
1,013 bar) du système binaire eau/éthanol,
fourni ci-dessous, pour répondre aux
questions suivantes. On désigne par xB et
yB la fraction molaire de l’eau
respectivement dans le liquide et dans la
vapeur. Sur le diagramme, indiquer avec
soin les constructions qui permettent de
répondre aux questions posées.
xB ou yB
1. Comment s’appelle le point du diagramme de coordonnées xB = 0,11 et T = 78,3°C ?
2. Préciser sur le diagramme les positions des courbes d’ébullition et de rosée ainsi que la nature des
phases présentes dans les différents domaines.
On considère une mole d’un mélange liquide de fraction molaire xB = 0,8, initialement à 20°C, que l’on chauffe
sous une pression constante de 1,013 bar.
3. A quelle température Teb exprimée en degré Celsius l’ébullition commence-t-elle et quelle est la fraction
molaire en alcool yA de la première bulle formée ?
4. A quelle température Tev la dernière goutte de liquide s’évapore-t-elle et quelle est la fraction molaire en
alcool xA dans cette dernière goutte ?
5. On place à 80°C une mole d’un mélange équimolaire d’eau et d’éthanol. A l’aide du diagramme isobare,
déterminer numériquement :
a. Les fractions molaires xA, yA, xB , yB en éthanol et en eau dans les deux phases.
b. Les quantités (en mol) de liquide et de gaz en présence, en expliquant la méthode employée.
c. Les quantités (en mol) d’éthanol dans les deux phases gazeuse et liquide (notées nA,V et nA,L) ainsi
que les quantités d’eau dans les deux phases gazeuse et liquide (notées nB,V et nB,L).
d. Le volume total de la phase gazeuse qui sera assimilée à un gaz parfait (on rappelle la valeur de la
constante des gaz parfaits : R = 8,314 J.mol-1.K-1).
6. Quelles sont les conséquences pratiques de l’existence du point minimum commun aux deux courbes
d’ébullition et de rosée sur la distillation des mélanges eau/éthanol ? Quelle est la composition du
distillat récupéré ?
7. On chauffe progressivement un mélange eau / éthanol de fraction molaire xB = 0,11 initialement à la
température de 20°C, en enregistrant la température. Représenter qualitativement la courbe donnant
l’évolution de la température en fonction du temps, en faisant apparaître clairement les domaines
monophasés et biphasés.
Philippe APLINCOURT
Master 1 MEEF Physique-Chimie
Equilibre liquide-solide du binaire eau-urée
On donne ci-dessous, le diagramme de cristallisation du binaire eau-urée, sous la pression atmosphérique.
1. Indiquer si l’urée et l’eau sont totalement miscibles ou non miscibles à l’état solide.
2. Nommer les courbes 1 et 2 séparant les différents domaines.
3. Indiquer à quelles compositions correspondent les domaines I à IV.
4. Comment se nomme le point A commun des deux courbes ? Préciser à quel système il correspond.
Un système est constitué d’une masse m1 = 70 g d’urée et d’une masse m2 = 30 g d’eau. Il est porté à 90°C. On
le refroidit régulièrement, sous la pression atmosphérique, jusqu’à une température de -30°C.
5. Tracer l’allure de la courbe d’analyse thermique donnant l’évolution de la température du système en
fonction du temps. Préciser les phénomènes se produisant aux différents points particuliers de la courbe.
Calculer la variance du système pour les domaines où plusieurs phases coexistent.
6. Rechercher la composition et calculer les masses de chaque phase pour une température de 0°C. Donner
la masse d’urée et la masse d’eau de la phase liquide.
Une masse m3 = 10 g d’urée solide pure est portée à -5°C. À pression et température constantes, on apporte petit
à petit une masse m4 = 90 g d’eau au système.
7. Selon la fraction massique globale en urée du système, indiquer la nature des phases en présence et la
fraction massique en urée de l’éventuelle phase liquide.
Philippe APLINCOURT
Master 1 MEEF Physique-Chimie
Mélange cuivre-argent
Dans le cas du mélange argent-cuivre, on observe une solubilité partielle à l’état solide.
On donne les points caractéristiques du diagramme binaire isobare (P = P0) argent-cuivre ; x(Cu) représente la
fraction atomique en cuivre du mélange.
Ag Cu
1400
1300
1200
Température (K)
1100
1000
900
800
700
600
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1
x (Cu)
1. Reproduire schématiquement le diagramme en reliant les points de façon appropriée. Préciser les
espèces (nature et état physique) présentes dans les différents domaines du diagramme ainsi définis et
préciser les coordonnées du point eutectique.
On laisse refroidir lentement un mélange argent-cuivre avec x(Cu) = 0,2 de 1400 K à 800 K.
2. Tracer l’allure de la courbe donnant la température du système en fonction du temps (courbe d’analyse
thermique) et préciser la variance du système au cours de la transformation.
3. Déterminer la composition du système à 1100 K.
On considère un barreau d’argent contenant 10% de cuivre considéré comme une impureté.
4. En vous aidant du diagramme, proposer une méthode de purification du barreau d’argent.
Philippe APLINCOURT
Master 1 MEEF Physique-Chimie
L’alliage aluminium/hafnium
L’aluminium s’allie à de nombreux composés. Sa légèreté et son coût modéré le rendent particulièrement
intéressant pour certaines applications où un poids élevé est un handicap, comme en aéronautique.
Le hafnium a la particularité de ne pas laisser passer les neutrons d’où les applications dans l’industrie
nucléaire pour arrêter les réacteurs. Du fait aussi de sa haute température de fusion, il est utilisé dans les
briques réfractaires. Avec l’aluminium, il rentre dans la composition de nouveaux alliages, comme les alliages
« superplastiques » au zirconium.
On s’intéresse ici au système binaire aluminium / hafnium (de symbole Hf). On désire construire le diagramme
isobare de cristallisation de ce système binaire sachant que les solides sont tous non miscibles entre eux et que
le liquide est homogène. Pour cela, on étudie les courbes de refroidissement de différents mélanges aluminium –
hafnium avec une fraction molaire d’aluminium comprise entre 0,60 et 0,75. Les différentes courbes sont
rassemblées sur la figure ci-dessous.
1. A l’aide de ces courbes, tracer le diagramme binaire isobare T(x) du système aluminium – hafnium pour
une fraction molaire x en aluminium comprise entre 0,60 et 0,75 et une température comprise entre
1480°C et 1720°C.
2. Pour chaque domaine du diagramme binaire, donner la nature des phases en présence. Indiquer le ou les
composés définis trouvés dans cette partie du diagramme binaire.
3. Pour x = 0,62 et x = 0,72, on observe un point particulier. Comment s’appelle ce point ? Quelle
particularité possède le mélange liquide à cette fraction molaire ?
4. Pour les courbes de refroidissement où x = 0,60, x = 0,62 et x = 0,69, décrire ce qu’il se passe, et
calculer la variance du système pour chaque partie de ces courbes.













